Человечество знакомо с калием больше полутора веков. В лекции, прочитанной в Лондоне 20 ноября 1807 г. Хэмфри Дэви сообщил, что при электролизе едкого калия он получил «маленькие шарики с сильным металлическим блеском... Некоторые из них сейчас же после своего образования сгорали со взрывом». Это и был калий .
Калий - замечательный металл . Замечателен он не только потому, что режется ножом, плавает в воде, вспыхивает на ней со взрывом и горит, окрашивая пламя в фиолетовый цвет. И не только потому, что этот элемент - один из самых активных химически. Все это можно считать естественным, потому что соответствует положению щелочного металла калия в таблице Менделеева. Калий замечателен своей незаменимостью для всего живого и примечателен как всесторонне «нечетный» металл.
Обратите внимание: его атомный номер 19, атомная масса 39, во внешнем электронном слое - один электрон, валентность 1+ . Как считают химики, именно этим объясняется исключительная подвижность калия в природе. Он входит в состав нескольких сотен минералов . Он находится в почве, в растениях, в организмах людей и животных. Он - как классический Фигаро: здесь - там - повсюду.
Калий и почва
Вряд ли можно объяснить случайностью или прихотью лингвистов тот факт, что в русском языке одним словом обозначаются и сама наша планета, и ее верхний слой - почва. «Земля-матушка», «земля-кормилица» - это, скорее, о почве, чем о планете в целом...
Но что такое почва? Самостоятельное и весьма своеобразное природное тело. Оно образуется из поверхностных слоев разнообразных горных пород под действием воздуха, воды, температурных перепадов, жизнедеятельности всевозможных обитателей Земли. Ниже, под почвой, скрыты так называемые материнские горные породы, сложенные из различных минералов. Они постепенно разрушаются и пополняют «запасы» почвы. А в почве, помимо чисто механического, постоянно происходит и другое разрушение. Его называют химическим выветриванием. Вода и углекислый газ (в меньшей мере другие вещества) постепенно разрушают минералы.
Почти 18% веса земной коры приходится на долю калийсодержащего минерала - ортоклаза . Это двойная соль кремневой кислоты K 2 Al 2 Si 6 O 16 или K 2 O-Al 2 O 3 -BSiO 2 . Вот что происходит с ортоклазом в результате химического выветривания:
K 2 O*AI 2 O 3 *6SO 2 + 2Н 2 О + CO 2 → K 2 CO 3 + Al 2 O 3 *2SO 2 *2H 2 O + + 4SiO 2 .
Ортоклаз превращается в каолин (разновидность глины), песок и поташ. Песок и глина идут на построение минерального костяка почвы, а K, перешедший из ортоклаза в поташ, «раскрепощается», становится доступным для растений. Но не весь сразу.
В почвенных водах молекулы K 2 CO 3 диссоциируют: К 2 СO 3 ↔ + К + + КСO 3 - ↔ 2К + + CO 3 2- . Часть ионов калия остается в почвенном растворе, который для растений служит источником питания. Но большая часть ионов калия поглощается коллоидными частицами почвы, откуда корням растений извлечь их довольно трудно. Вот и получается, что, хотя калия в земле много, часто растениям его не хватает. Из-за того, что комочки почвы «запирают» большую часть калия, содержание этого элемента в морской воде почти в 50 раз меньше, чем натрия. Подсчитано, что из тысячи атомов калия, освобождающихся при химическом выветривании, только два достигают морских бассейнов, а 998 остаются в почве. «Почва поглощает калий, и в этом ее чудодейственная сила», - писал академик А. Е. Ферсман.
Калий и растения
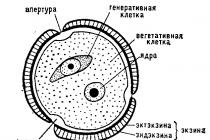
Калий содержится во всех растениях . Отсутствие калия приводит растение к гибели. Почти весь калий находится в растениях в ионной форме - K + . Часть ионов находится в клеточном соке, другая часть поглощена структурными элементами клетки. Ионы калия участвуют во многих биохимических процессах, происходящих в растении. Установлено, что в клетках растений эти ионы находятся главным образом в протоплазме. В клеточном ядре они не обнаружены. Следовательно, в процессах размножения и в передаче наследственных признаков элемент № 19 не участвует. Но и без этого роль калия в жизни растения велика и многообразна.
Калий входит и в плоды, и в корни, и в стебли, и в листья, причем в вегетативных органах его, как правило, больше, чем в плодах. Еще одна характерная особенность: в молодых растениях больше калия, чем в старых. Замечено также, что по мере старения отдельных органов растений ионы калия перемещаются в точки наиболее интенсивного роста. При недостатке калия растения медленнее растут, их листья, особенно старые, желтеют и буреют по краям, стебель становится тонким и непрочным, а семена теряют всхожесть.
Установлено, что ионы калия активизируют синтез органических веществ в растительных клетках. Особенно сильно влияют они на процессы образования углеводов. Если калия не хватает, растение хуже усваивает углекислый газ, и для синтеза новых молекул углеводов ему недостает углеродного «сырья». Одновременно усиливаются процессы дыхания, и сахара, содержащиеся в клеточном соке, окисляются. Таким образом, запасы углеводов в растениях, оказавшихся на голодном пайке (по калию), не пополняются, а расходуются. Плоды такого растения - это особенно заметно на фруктах - будут менее сладкими, чем у растений, получивших нормальную дозу калия. Крахмал - тоже углевод, поэтому и на его содержание в плодах сильно влияет элемент № 19.
Но и это не все. Растения, получившие достаточно калия, легче переносят засуху и морозные зимы. Это объясняется тем, что элемент № 19 влияет на способность коллоидных веществ растительных клеток поглощать воду и набухать. Не хватает калия - клетки хуже усваивают и удерживают влагу, сжимаются, отмирают.
Ионы калия влияют и на азотный обмен веществ. При недостатке калия в клетках накапливается избыток аммиака. Это может привести к отравлению и гибели растения.
Уже упоминалось, что K влияет и на дыхание растений, а усиление дыхания сказывается не только на содержании углеводов. Чем интенсивнее дыхание, тем активнее идут все окислительные процессы, и многие органические вещества превращаются в органические кислоты. Избыток кислот может вызвать распад белков. Продукты этого распада - весьма благоприятная среда для грибков и бактерий. Вот почему при калийном голодании растения намного чаще поражаются болезнями и вредителями. Фрукты и овощи, содержащие продукты распада белков, плохо переносят транспортировку, их нельзя долго хранить.Одним словом, хочешь получать вкусные и хорошо сохраняющиеся плоды - корми растение калием вволю. А для зерновых калий важен еще по одной причине: он увеличивает прочность соломы и тем самым предупреждает полегание хлебов...
- ВСТРЕЧА С КАЛИЕМ? Если на складе или на товарной станции вы увидите стальные ящики с надписями: «Огнеопасно!», «От воды взрывается», то весьма вероятно, что вы встретились с калием.
Много предосторожностей предпринимают при перевозке этого металла. Поэтому, вскрыв стальной ящик, вы не увидите калия, а увидите тщательно запаянные стальные банки. В них - калий и инертный газ - единственная безопасная для калия среда. Большие партии калия перевозят в герметических контейнерах под давлением инертного газа, равным 1,5 атм.
- ЗАЧЕМ НУЖЕН МЕТАЛЛИЧЕСКИЙ КАЛИЙ? Металлический K используют как катализатор в производстве некоторых видов синтетического каучука, а также в лабораторной практике. В последнее время основным применением этого металла стало производство перекиси калия K 2 O 2 , используемой для регенерации кислорода . Сплав калия с натрием служит теплоносителем в атомных реакторах, а в производстве титана - восстановителем.
- ИЗ СОЛИ И ЩЕЛОЧИ. Получают элемент №19 чаще всего в обменной реакции расплавленных едкого калия и металлического натрия: KOH + Na → NaOH + K. Процесс идет в ректификационной колонне из никеля при температуре 380-440°С. Подобным образом получают элемент № 19 и из хлористого калия, только в этом случае температура процесса выше - 760-800°С. При такой температуре и натрий, и калий превращаются в пар, а хлористый калий (с добавками) плавится. Пары натрия пропускают через расплавленную соль и конденсируют полученные пары калия. Этим же способом получают и сплавы натрия с калием. Состав сплава в большой мере зависит от условий процесса.
- КАК БЫТЬ, ЕСЛИ вы впервые имеете дело с металлическим калием. Необходимо помнить о высочайшей реакционной способности этого металла, о том, что калий воспламеняется от малейших следов воды. Работать с калием обязательно в резиновых перчатках и защитных очках, а лучше - в маске» закрывающей все лицо. С большими количествами калия работают в специальных камерах, заполненных азотом или аргоном. (Разумеется, в специальных скафандрах.) А если K все-таки воспламенился, его тушат не водой, а содой или поваренной солью.
- КАК БЫТЬ С ОТХОДАМИ. Правила безопасности категорически запрещают накапливать в лабораториях больше двух граммов остатков или отходов какого-либо щелочного металла, калия в том числе. Отходы подлежат уничтожению на месте. Классический способ - образование под действием этилового спирта этилата калия C 2 H 5 OK: просто льют в отходы спирт. Но есть и другой - безспиртовой способ. Отходы заливают керосином или бензином. Калий с ними не реагирует и, будучи легче воды, но тяжелее этих органических жидкостей, оседает на дно. И тогда в наклоненный сосуд начинают по каплям добавлять воду. Когда вода доберется до металла, произойдет реакция и K превратится в едкое кали. Слои щелочного раствора и керосина или бензина довольно легко разделяются на делительной воронке.
- ЕСТЬ ЛИ В РАСТВОРЕ ИОНЫ КАЛИЯ? Выяснить это несложно. Проволочное колечко опустите в раствор, а затем внесите в пламя газовой горелки. Если калий есть, пламя окрасится в фиолетовый цвет, правда, не в такой яркий, как желтый цвет, придаваемый пламени соединениями натрия. Сложнее определить, сколько калия в растворе. Нерастворимых в воде соединений у этого металла немного. Обычно калий осаждают в виде перхлората - соли очень сильной хлорной кислоты HClO 4 . Кстати, перхлорат калия - очень сильный окислитель и в этом качестве применяется в производстве некоторых взрывчатых веществ и ракетных топлив.
- ДЛЯ ЧЕГО НУЖЕН ЦИАНИСТЫЙ КАЛИЙ? Для извлечения золота и серебра из руд. Для гальванического золочения и серебрения неблагородных металлов. Для получения многих органических веществ. Для азотирования стали - это придает ее поверхности большую прочность. К сожалению, это очень нужное вещество чрезвычайно ядовито. А выглядит KCN вполне безобидно: мелкие кристаллы белого цвета с коричневатым или серым оттенком.
- ЧТО ТАКОЕ ХРОМПИК? Точнее - хромпик калиевый. Это оранжевые кристаллы состава K 2 Cr 2 O 7 . Хромпик используют в производстве красителей, а его растворы - для «хромового» дубления кож, а также в качестве протравы при окраске и печатании тканей. Раствор хромпика в серной кислоте - хромовая смесь, которую во всех лабораториях применяют для мытья стеклянной посуды.
- ЗАЧЕМ НУЖНО ЕДКОЕ КАЛИ? В самом деле, зачем? Ведь свойства этой щелочи и более дешевого едкого натра практически одинаковы. Разницу между этими веществами химики обнаружили лишь в XVIII в. Самое заметное различие между NaOH и KOH в том, что едкое кали в воде растворяется еще лучше, чем едкий натр. KOH получают электролизом растворов хлористого калия. Чтобы примесь хлоридов была минимальной, используют ртутные катоды. А нужно это вещество прежде всего как исходный продукт для получения различных солей калия. Кроме того, без едкого кали не обойтись в производстве жидких мыл, некоторых красителей и органических соединений. Раствор едкого кали используется в качестве электролита в щелочных аккумуляторах.
- СЕЛИТРА ИЛИ СЕЛИТРЫ? Правильнее - селитры. Это общее название азотнокислых солей щелочных и щелочноземельных металлов. Если же говорят просто «селитра» (не «натриевая» или «кальциевая» или «аммиачная», а просто - «селитра»), то имеют в виду нитрат калия. Этим веществом человечество пользуется уже больше тысячи лет - для получения черного пороха. Кроме того, селитра - первое двойное удобрение: из трех важнейших для растений элементов в ней есть два - азот и калий. Вот как описал селитру Д. И. Менделеев в «Основах химии»:
«Селитра представляет бесцветную соль, имеющую особый прохладительный вкус. Она легко кристаллизуется длинными, по бокам бороздчатыми, ромбическими, шестигранными призмами, оканчивающимися такими же пирамидами. Ее кристаллы (уд. вес 1,93) не содержат воды. При слабом накаливании (339°) селитра плавится в совершенно бесцветную жидкость. При обыкновенной температуре в твердом виде KNO 3 малодеятельна и неизменна, но при возвышенной температуре она действует как весьма сильное окисляющее средство, потому что может отдать смешанным с нею веществам значительное количество кислорода. Брошенная на раскаленный уголь селитра производит быстрое его горение, а механическая смесь ее с измельченным углем загорается от прикосновения с накаленным телом и продолжает сама собою гореть. При этом выделяется азот, а кислород селитры идет на окисление угля, вследствие чего и получаются углекалиевая соль и углекислый газ...
В химической практике и технике селитра употребляется во многих случаях как окислительное сродство, действующее при высокой температуре. На этом же основано применение ее для обыкновенного пороха, который есть механическая смесь мелко измельченных: серы, селитры и угля».
- ГДЕ И ДЛЯ ЧЕГО ПРИМЕНЯЮТСЯ ПРОЧИЕ СОЛИ КАЛИЯ? Бромистый калий KBr - в фотографии, чтобы предохранить негатив или отпечаток от вуали.
- Йодистый калий KI - в медицине и как химический реактив.
- Фтористый калий KF - в составе металлургических флюсов и для введения фтора в органические соединения.
- Углекислый калий (поташ) K 2 CO 3 - в стекольном и мыловаренном производствах, а также как удобрение.
- Фосфаты калия, в частности K 4 P 2 O 7 и K 5 P 3 O 10 , - как компоненты моющих средств.
- Хлорат калия (бертолетова соль) KClO 3 - в спичечном производстве и пиротехнике.
- Кремнефтористый калий K 2 SiF 6 - как добавка к шихте при извлечении редкоземельных элементов из минералов.
- Железистосинеродистый калий (желтая кровяная соль) K 4 Fe(CN) 6 -SH 2 O - как протрава при крашении тканей и в фотографии.
- ПОЧЕМУ КАЛИЙ НАЗВАЛИ КАЛИЕМ? Слово это арабского происхождения. По-арабски, «аль-кали» - зола растений. Впервые калий получен из едкого кали, а едкое кали - из поташа, выделенного из золы растений... Впрочем, в английском и других европейских языках сохранилось название potassium, данное калию его первооткрывателем X. Дэви. В русскую химическую номенклатуру название «калий» введено в 1831 г. Г. И. Гессом.
- ОТНЮДЬ HE ТОЛЬКО В КУРАГЕ. Сердечникам, в первую очередь людям, перенесшим инфаркт, для восполнения потерь калия в организме настоятельно рекомендуют есть курагу. Или в крайнем случае изюм. В 100 граммах кураги до 2 г калия. Столько же ее в урюке (но для точности при расчете надо вычесть вес косточек). Изюм содержит калия примерно вдвое меньше. Но не надо думать, будто сухофрукты - единственный источник калия. Его довольно много почти в любой растительной пище. Например, сорок граммов жареного картофеля эквивалентны 10 граммам отборной кураги. Богаты калием бобовые, чай, порошок какао. Одним словом, суточную дозу калия (2,5-5 г) при нормальном питании получить нетрудно.
Калий — обозначается символом K — химический элемент I группы периодической системы Менделеева;
- атомный номер 19,
- атомная масса 39,098;
Калий — серебристо-белый, очень легкий, мягкий и легкоплавкий металл.
Элемент состоит из двух стабильных изотопов — 39K (93,08%), 41K (6,91%) и одного слабо радиоактивного 40K (0,01%) с периодом полураспада 1,32·109 лет.
Элемент калий находится в четвертом периоде периодической системы, значит, все электроны располагаются на четырех энергетических уровнях. Таким образом, строение атома калия записывается так: +19 К: 2ё; 8ё; 8ё; 1ё.
Исходя из строения атома, можно предсказать степень окислени С1 калия в его соединениях. Так как в химических реакциях атом калия отдает один внешний электрон, проявляя восстановительные свойства, следовательно, он приобретает степень окисления +1.

Восстановительные свойства у калия выражены сильнее, чем у натрия, но слабее, чем у рубидия, что связано с ростом радиусов от Nа к Rb.
Калий - простое вещество, для него характерна металлическая кристаллическая решетка и металлическая химическая связь, а отсюда - и все типичные для металлов свойства.
Металлические свойства у калия выражены сильнее, чем у натрия, но слабее, чем у рубидия, т.к. атом калия легче отдает электрон, чем атом натрия, но труднее, чем атом рубидия.
Металлические свойства у калия выражены сильнее, чем у кальция, т.к. один электрон атома калия легче оторвать, чем два электрона атома кальция.
Оксид калия К 2 O является основным оксидом и проявляет все типичные свойства основных оксидов. Взаимодействие с кислотами и кислотными оксидами.
К 2 O + 2НСl = 2КСl +H 2 O;
К 2 O +SO 3 = К 2 SO 4
В качестве гидроксида калию соответствует основание (щелочь) КОН, которое проявляет все характерные свойства оснований: взаимодействие с кислотами и кислотными оксидами.
КОН+НNОз = КNO 3 +Н 2O ;
2КОН+H 2 O 5 = 2KNO 3 +Н 2 O.
Летучего водородного соединения калий не образует, а образует гидрид калия КН
В природе калий встречается только в соединениях с другими элементами, например, в морской воде, а также во многих минералах. Он очень быстро окисляется на воздухе и очень легко вступает в химические реакции, особенно с водой, образуя щёлочь. Во многих отношениях химические свойства калия очень близки к натрию, но с точки зрения биологической функции и использования их клетками живых организмов они все же отличаются.
Калием называется элемент, находящийся в периодической системе Менделеева под 19-ым номером. Вещество принято обозначать заглавной буквой К (от латинского Kalium). В русской химической номенклатуре настоящее название элемента появилось благодаря Г.И. Гессу в 1831 году. Изначально калий называли «аль-кали», что в переводе с арабского означает «зола растений». Именно едкий кали стал материалом для самого первого получения вещества. Едкий кали, в свою очередь, добывался из поташа, который являлся продуктами горения растений (карбонат калия). Его первооткрывателем стал Х. Дэви. Стоит отметить, что карбонат калия является прототипом современного моющего средства. Позже он использовался для удобрений, используемых в сельском хозяйстве, в производстве стекла и других целей. В настоящее поташ - это пищевая добавка, прошедшая официальную регистрацию, а калий научились добывать совершенно другими путями.
В природе калий можно обнаружить только в виде соединений с другими элементами (например, морская вода, или минералы), свободный его вид не встречается вообще. Он способен в достаточно короткий промежуток времени окисляться на открытом воздухе, а также вступать в химические реакции (например, при взаимодействии калия с водой, образуется щелочь).
| Страна, часть света | Запасы общие | Запасы подтвержденные | Их % от мира | Среднее содержание |
|---|---|---|---|---|
| 1 | 2 | 3 | 4 | 5 |
| Россия | 19118 | 3658 | 31,4 | 17,8 |
| Европа | 3296 | 2178 | 18,5 | - |
| Беларусь | 1568 | 1073 | 9,1 | 16 |
| Великобритания | 30 | 23 | 0,2 | 14 |
| Германия | 1200 | 730 | 6,2 | 14 |
| Испания | 40 | 20 | 0,2 | 13 |
| Италия | 40 | 20 | 0,2 | 11 |
| Польша | 10 | 10 | 0,1 | 12 |
| Украина | 375 | 292 | 2,5 | 11 |
| Франция | 33 | 10 | 0,1 | 15 |
| Азия | 2780 | 1263 | 10,8 | - |
| Израиль | 600 | 44 | 0,4 | 1,4 |
| Иордания | 600 | 44 | 0,4 | 1,4 |
| Казахстан | 102 | 54 | 0,5 | 8 |
| Китай | 320 | 320 | 2,7 | 12 |
| Таиланд | 150 | 75 | 0,6 | 2,5 |
| Туркменистан | 850 | 633 | 5,4 | 11 |
| Узбекистан | 159 | 94 | 0,8 | 12 |
| Африка | 179 | 71 | 0,6 | - |
| Конго | 40 | 10 | 0,1 | 15 |
| Тунис | 34 | 19 | 0,2 | 1,5 |
| Эфиопия | 105 | 42 | >0,4 | 25 |
| 14915 | 4548 | 38,7 | - | |
| Аргентина | 20 | 15 | 0,1 | 12 |
| Бразилия | 160 | 50 | 0,4 | 15 |
| Канада | 14500 | 4400 | 37,5 | 23 |
| Мексика | 10 | - | 0 | 12 |
| США | 175 | 73 | 0,6 | 12 |
| Чили | 50 | 10 | 0,1 | 3 |
| Итого: | 40288 | 11744 | 100 | - |
Описание калия
Калий в виде простого вещества представляет собой щелочной металл. Для него характерен серебристо-белый окрас. На свежей поверхности моментально появляется блеск. Калий является мягким металлом, легко поддающимся плавлению. Если вещество или его соединения поместить в пламя горелки, то огонь приобретет розово-фиолетовый цвет.
Физические свойства калия
Калий очень мягкий металл, который легко разрезать обычным ножом. Его твердость по Бринеллю составляет 400 кн/м 2 (или 0,04 кгс/мм 2). Он имеет объемноцентрированную кубическую кристаллическую решетку (5=5,33 А). Его плотность составляет 0,862 г/см 3 (20 0 С). Вещество начинает плавиться при температуре в 63,55 0 С, закипать - при 760 0 С. Имеет коэффициент термического расширения, который равняется 8,33*10 -5 (0-50 0 С). Его удельная теплоемкость при температуре в 20 0 С составляет 741,2 дж/(кг*К) или же 0,177 кал/(г* 0 С). При той же температуре имеет удельное электросопротивление, равное 7,118*10 -8 ом*м. Температурный коэффициент электросопротивления металла составляет 5,8*10 -15 .
Калий образует кристаллы кубической сингонии, пространственная группа I m3m, параметры ячейки a = 0,5247 нм, Z = 2.
Химические свойства
Калий является щелочным металлом. В связи с этим, металлические свойства калия проявляются типично, так же, как и других подобных металлов. Элемент проявляет свою сильную химическую активность, а кроме этого, также выступает в роли сильного восстановителя Как уже говорилось выше, металл активно вступает в реакцию с воздухом, о чем свидетельствует появление пленок на его поверхности, в результате чего его цвет становится тусклым. Данную реакцию можно наблюдать невооруженным глазом. Если калий на протяжении достаточно длительного времени контактирует с атмосферой, то есть вероятность его полного разрушения. При вступлении в реакцию с водой, происходит характерный взрыв. Это связано с выделяющимся водородом, который воспламеняется характерным розовато-фиолетовым пламенем. А при добавлении в воду, реагирующую с калием фенолфталеина, она приобретает малиновый цвет, который свидетельствует о щелочной реакции образующегося гидроксида калия (КОН).
При взаимодействии металла с такими элементами, как Na, Tl, Sn, Pb, Bi, образуются интерметаллиды
Указанные характеристики калия говорят о необходимости соблюдений определенных правил безопасности и условий во время хранения вещества. Так, вещество следует покрывать слоем бензина, керосина или силикона. Это делается для полного исключения его контакта с воздухом или водой.
Стоит отметить, что в условиях комнатной температуры металл вступает в реакцию с галогенами. Если его немного нагреть, то он легко взаимодействует с серой. В случае же увеличения температуры, калий способен соединяться с селеном и теллуром. Если повысить температуру более 200 0 С в атмосфере водорода, то образуется гидрид КН, который способен воспламеняться без посторонней помощи, т.е. самостоятельно. Калий совершенно не взаимодействует с азотом, даже если для этого создать надлежащие условия (повышенные температуру и давление). Однако, контактировать эти два вещества можно заставить, повлияв на них электрическим разрядом. В данном случае получится азид калия KN 3 и нитрид калия K 3 N. Если нагреть вместе графит и калий, то в результате получатся карбиды KC 8 (при 300 °С) и KC 16 (при 360 °C).
При взаимодействии калия и спиртов получаются алкоголяты. Кроме этого, калий делает существенно быстрее процесс полимеризации олефинов и диолефинов. Галогеналкилы и галогенарилы вместе с девятнадцатым элементом в результате дают калийалкилы и калийарилы.
| Характеристика | Значение |
|---|---|
| Свойства атома | |
| Название, символ, номер | Калий / Kalium (K), 19 |
| Атомная масса (молярная масса) | 39,0983(1) а. е. м. (г/моль) |
| Электронная конфигурация | 4s1 |
|
Радиус атома |
235 пм |
| Химические свойства | |
| Ковалентный радиус | 203 пм |
| Радиус иона | 133 пм |
| Электроотрицательность | 0,82 (шкала Полинга) |
| Электродный потенциал | −2,92 В |
| Степени окисления | 0; +1 |
|
Энергия ионизации (первый электрон) |
418,5 (4,34) кДж/моль (эВ) |
| Термодинамические свойства простого вещества | |
| Плотность (при н. у.) | 0,856 г/см³ |
| Температура плавления | 336,8К; 63,65 °C |
| Температура кипения | 1047К; 773,85 °C |
| Уд. теплота плавления | 2,33 кДж/моль |
| Уд. теплота испарения | 76,9 кДж/моль |
| Молярная теплоёмкость | 29,6 Дж/(K·моль) |
| Молярный объём | 45,3 см³/моль |
| Кристаллическая решётка простого вещества | |
| Структура решётки | Кубическая объёмно-центрированная |
| Параметры решётки | 5,332 Å |
| Температура Дебая | 100 K |
Электронное строение атома калия
Калий имеет положительно заряженное ядро атома (+19). В середине этого атома присутствуют 19 протонов и 19 нейтронов, которые окружаются четырьмя орбитами, где в постоянном движении находятся 19 электронов. Электроны распределены на орбиталях в следующем порядке:
1s 2 2s 2 2p 6 3s 2 3p 6 4s 1 .
На внешнем энергетическом уровне атома металла находится всего 1 валентный электрон. Это объясняет тот факт, что абсолютно во всех соединениях калий имеет валентность 1. В отличие от лития и натрия, данный электрон располагается на более удаленном расстоянии от ядра атома. Это является причиной повышенной химической активностью калия, чего нельзя сказать об упомянутых двух металлах. Таким образом, внешняя электронная оболочка калия представлена следующей конфигурацией:
Не смотря на присутствие вакантных 3p - и 3d -орбиталей, возбужденное состояние отсутствует.
Калий - щелочной металл, который достаточно широко распространен на Земле. Соединения калия с давних времен знакомы людям. Элемент был открыт в 1807 году и был изначально назван потассием. Однако, название не прижилось и чуть позже элемент был назван калием.
С давних времен люди получали поташ (карбонат калия) из продуктов горения. Его использовали как моющее средство, чуть позже его начали применять для производства различных сельскохозяйственных удобрений, для изготовления стекла и других целей. На сегодняшний день поташ даже является официально зарегистрированной пищевой добавкой.
Характеристика калия
Физические свойства

Элемент имеет бледно-серебристый цвет. На только что образовавшейся поверхности возникает характерный блеск. Калий - легкий металл. Легко плавится. Его можно растворить в ртути, в результате этого процесса образуются амальгамы. Горит красновато-фиолетовым пламенем.
Химические свойства

Калий является металлом и обладает всеми соответствующими свойствами. Также элемент относится к группе щелочных. Этим и объясняется его повышенная химическая активность. Калий, реагируя с другими веществами, отдает электроны, является сильным восстановителем.
- Вступает в бурную реакцию с кислородом, образуя супероксид калия.
- При нагревании реагирует с водородом.
- Хорошо реагирует со всеми неметаллическими элементами, образуя при этом нитриды, фосфиды, сульфиды и другие соединения.
- Вступает в реакцию со многими сложными веществами: солями, оксидами, а также с водой. Реакция с водой протекает очень бурно, со взрывом.

Соединения калия достаточно распространены в природе. В чистом виде калий встретить нельзя. Причина этому - его повышенная химическая активность.
Где же в природе можно найти калий?
- Во-первых, калий в достаточно больших количествах содержится в коре Земли. Его содержание оценивается примерно в 2,4%. Калий является важной составляющей почвы, горных пород.
- Во-вторых, большие залежи солей калия зафиксированы на местах испарения древних морей.
- Также существенное количество калия содержат в себе воды Мирового океана. В водах Мирового океана концентрация калия составляет примерно 0,06%. В отдельных водоемах (например, Мертвое море), концентрация калия может быть и 1,5%. Такая повышенная концентрация делает экономически выгодной добычу калия. Так, в Иордании стоит завод по добыче калия из вод Мертвого моря.
Области применения калия

Сфера использования калия существенно уже по сравнению с тем же натрием. Это обусловлено тем, что калий обладает большей химической активностью. Кроме того, калий является более дорогим металлом. Тем не менее, калий все же используется в различных отраслях промышленности.
- Активней всего калий используют в химической промышленности для производства удобрений. Калий является важным элементом для растений. Довольно часто растения испытывают нехватку калия, что приводит к тому, что растение не может использовать весь свой потенциал роста. Растение становится ослабленным, медленнее растет, стебель слабеет, листья желтеют и опадают, семена становятся менее всхожими. Дефицит калия в таких случаях восполняют с помощью удобрений. Именно калийные удобрения являются основной продукцией, для которой используется калий. Самым распространенным калийным удобрением является хлорид калия (KCl).
- Кроме того, элемент и его соединения используют в машиностроении. Гидроксид калия - важнейший элемент для изготовления аккумуляторов.
- Соединения калия также используются в пищевой промышленности. Яркий пример - нитрат калия. Вещество является пищевой добавкой. Используется в качестве консерванта.

КАЛИЙ (лат. Kalium), K (читается «калий»), химический элемент с атомным номером 19, атомная масса 39,0983.
Калий встречается в природе в виде двух стабильных нуклидов: 39 К (93,10% по массе) и 41 К (6,88%), а также одного радиоактивного 40 К (0,02%). Период полураспада калия-40 Т 1/2 примерно в 3 раза меньше, чем Т 1/2 урана-238 и составляет 1,28 миллиарда лет. При b распаде калия-40 образуется стабильный кальций-40, а при распаде по типу электронного захвата образуется инертный газ аргон-40.
2K + 2H 2 O = 2KOH + H 2
8К + 4Н 2 SO 4 = K 2 S + 3K 2 SO 4 + 4H 2 O.
При нагревании до 200-300°C калий реагирует с водородом (H) с образованием солеподобного гидрида КН:
Получение: в настоящее время калий получают при взаимодействии с жидким натрием (Na) расплавленных KOH (при 380-450°C) или KCl (при 760-890°C):
Na + KOH = NaOH + K
Калий также получают электролизом расплава KCl в смеси с K 2 CO 3 при температурах, близких к 700°C:
2KCl = 2K + Cl 2
От примесей калий очищают вакуумной дистилляцией.
Применение: металлический калий материал для электродов в химических источниках тока. Сплав калия с другим щелочным металлом натрием (Na) находит применение в качестве теплоносителя в ядерных реакторах.
В гораздо больших масштабах, чем металлический калий, находят применение его соединения. Калий важный компонент минерального питания растений (на это уходит около 90% добываемых солей калия), он необходим им в значительных количествах для нормального развития, поэтому широкое применение находят калийные удобрения: хлорид калия КСl, нитрат калия, или калийная селитра, KNO 3 , поташ K 2 CO 3 и другие соли калия. Поташ используют также при производстве специальных оптических стекол, как поглотитель сероводорода при очистке газов, как обезвоживающий агент и при дублении кож.
В качестве лекарственного средства находит применение иодид калия KI. Иодид калия используют также в фотографии и в качестве микроудобрения. Раствор перманганата калия КMnO 4 («марганцовку») используют как антисептическое средство.
Биологическая роль: калий один из важнейших биогенных элементов , постоянно присутствующий во всех клетках всех организмов. Ионы калия К + участвуют в работе ионных каналов и регуляции проницаемости биологических мембран, в генерации и проведении нервного импульса, в регуляции деятельности сердца и других мышц, в различных процессах обмена веществ. Содержание калия в тканях животных и человека регулируется стероидными гормонами надпочечников. В среднем организм человека (масса тела 70 кг) содержит около 140 г калия. Поэтому для нормальной жизнедеятельности с пищей в организм должно поступать 2-3 г калия в сутки. Богаты калием такие продукты, как изюм, курага, горох и другие.